
Le rôle de CRISPR dans l’ingénierie du microbiome [Podcast]
Rôle de CRISPR dans les avancées scientifiques de l’ingénierie du microbiome
Les répétitions palindromiques courtes groupées régulièrement espacées (CRISPR) ont été découvertes pour la première fois dans le génome des bactéries marines. Face à une menace virale, les cellules bactériennes ont développé une réponse immunitaire en capturant et copiant des fragments d’ADN de virus. Cela a permis aux bactéries de reconnaître les attaques ultérieures et de cliver l’ADN viral pour arrêter l’infection virale. Il a également été découvert que l’enzyme Cas était responsable du clivage de l’ADN. Ce mécanisme de défense a ensuite été exploité par Doudna et Charpentier, qui pouvaient cibler une séquence d’ADN spécifique et l’isoler à l’aide du système CRISPR-Cas9 (1).
Au cours de la dernière décennie, CRISPR-Cas9 s’est avéré extrêmement précieux dans la découverte et la fabrication de médicaments. En utilisant un ARN guide synthétique (ARNg), les chercheurs peuvent cibler une séquence d’ADN spécifique et utiliser Cas9 pour la découper. Par la suite, la machine de réparation hôte essaie de réparer l’ADN par une jonction d’extrémité non homologue (NHEJ), conduisant à des mutations aléatoires qui altèrent la fonction génétique. Grâce à ce mécanisme, les chercheurs peuvent désormais réduire en silence les gènes pour élucider leurs rôles dans le phénotype de la maladie, ce qui peut être bénéfique pour la découverte de cibles. En outre, les chercheurs peuvent également utiliser CRISPR-Cas9 pour révéler les mécanismes de résistance aux médicaments en identifiant l’ensemble des gènes associés à l’évasion du système immunitaire.
Aujourd’hui, cependant, nous allons explorer une application différente de CRISPR : Ingénierie du microbiome. Proposé par Molecular Devices, l’épisode récent du podcast Drug Target Reviews aborde les applications de CRISPR dans l’ingénierie du microbiome et la manière dont il peut surmonter le goulot d’étranglement de la recherche sur le microbiome humain.
Rejoignez les principaux experts Dr Jakob Haaber , Vice-président et Responsable des technologies de livraison, SNIPR Biome et Dr Richard Fox , Cofondateur, PDG et Directeur technique d’Infinome Biosciences, qui discuteront du large éventail d’utilisations pour CRISPR, y compris pour les produits thérapeutiques et la biofabrication.
Comment CRISPR-Cas9 aide à étudier le rôle du microbiome humain dans les maladies
Il est maintenant bien connu que le corps humain contient des billions de micro-organismes, dépassant ainsi le nombre de cellules humaines. Collectivement appelés microbiomes, ces micro-organismes forment une symbiose avec l’organisme en régulant l’environnement extracellulaire et en protégeant les cellules contre les pathogènes. Il n’est donc pas surprenant que les perturbations du microbiome soient étroitement associées à de nombreuses maladies, du diabète à l’obésité en passant par le cancer.
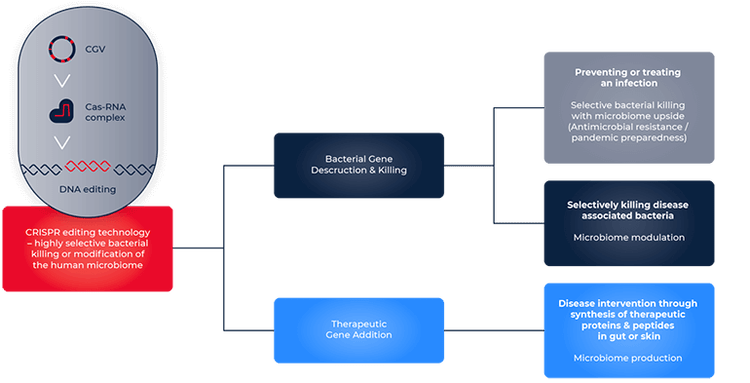
Avantages de CRISPR et développements récents
Selon Richard Fox, cofondateur, PDG et directeur technique d’Infinome Biosciences, la principale force de CRISPR vient de sa capacité à intensifier l’édition génomique. « Au lieu de mutations aléatoires sur un petit ensemble de gènes cibles, nous pouvons désormais modifier avec précision une voie ou un génome entier, introduisant des centaines de milliers de changements. »
L’édition génomique à grande échelle donne lieu à des banques de cellules disponibles dans le commerce que les chercheurs peuvent intégrer dans un criblage phénotypique haut débit. Ces banques éliminent la nécessité d’éliminer manuellement un grand nombre de gènes pour le profilage phénotypique et proposent une solution pour l’accélération des études de découverte de médicaments.
Un autre avantage des technologies CRISPR est leur spécificité améliorée. L’édition génétique du microbiome est l’un des domaines qui présente les avantages de la spécificité. Les systèmes CRISPR peuvent être programmés pour couper de l’ADN bactérien spécifique ou même éliminer des circuits génétiques dans les parois cellulaires bactériennes sans tuer la cellule. Ensemble, ces avancées conduisent à de nouvelles thérapies géniques pour les écarts du microbiote intestinal.
En attendant, les systèmes CRISPR ont permis la fabrication de constructions génétiques plus petites pour faciliter l’emballage dans les véhicules de livraison. Ainsi, le véhicule d’administration peut transporter plusieurs composants en plus de CRISPR, constituant un agent thérapeutique multifonctionnel à base de gènes qui accomplit bien plus que la simple découpe ou l’insertion d’ADN.
Accélération de la fabrication des technologies CRISPR
L’écart entre la biologie de synthèse et la bio-ingénierie est souvent causé par des problèmes de temps et de coût. La mise sur le marché d’une solution de biofabrication nécessite de grandes entités avec une infrastructure bien construite, une automatisation robuste, de nombreuses personnes, des instruments, des systèmes informatiques et beaucoup de capital. Il n’est donc pas surprenant que le développement d’agents biologiques puisse prendre 5à10 ans et plusieurs millions de dollars. Il s’agit d’un investissement assez risqué, donc les entreprises pharmaceutiques hésitent souvent à y participer, laissant des territoires avec un énorme potentiel thérapeutique inexploré.
La configuration du système d’édition génomique activé par CRISPR est l’un des goulots d’étranglement des flux de travail. La conception de systèmes d’ingénierie génomique à grande échelle est assez laborieuse, car il peut être nécessaire de produire de minuscules quantités de séquence de donneurs pour cibler et modifier précisément les 10 000 loci dans un génome entier.
L’un des cofondateurs d’Infinome Biosciences, Andrew Garst, a mis au point une innovation clé en associant la séquence guide qui dirige la coupe à la séquence de donneurs qui médie la réparation, réduisant ainsi l’édition du génome large à seulement quelques clics. Richard Fox estime que « de tels systèmes automatisés de conception et de construction peuvent créer des bibliothèques cellulaires modifiées en moins d’une semaine, ce qui représente la fraction de l’effort qu’il prenait auparavant ».
Étapes de l’édition des gènes microbiens
La première étape de l’édition génétique pour le microbiome intestinal est la validation in vitro du système CRISPR. La spécificité de l’édition CRISPR est testée par rapport à un ensemble de panels bactériens représentatifs du microbiome intestinal. L’objectif est de s’assurer que le système CRISPR cible une sous-espèce prédéterminée de bactéries et que les bactéries bénéfiques sont exemptées de l’édition génétique induite par CRISPR.
Ensuite, la validation se poursuit avec les études précliniques et cliniques. En utilisant des techniques de séquençage génomique, les chercheurs démontrent que l’édition génétique ne perturbe pas le microbiome de manière nocive. Bien sûr, des effets hors cible pourraient inévitablement se produire, comme le révèle le séquençage du génome entier. La marche à suivre consiste à surveiller le taux d’occurrence et à s’assurer que ces effets sont mineurs et n’interfèrent pas avec l’édition génétique.
Le séquençage et le profilage phénotypique révèlent l’ensemble des modifications qu’un génome porte, ainsi que les souches prédominantes dans une population bactérienne. Pour valider davantage le succès de l’édition génomique ciblée, on peut soumettre la population bactérienne à des facteurs de stress environnementaux et surveiller leur comportement. Cela garantit que l’édition génétique confère aux bactéries les propriétés souhaitées, par exemple la capacité à se développer sous un stress environnemental tel qu’une hypoxie.

Grâce aux flux de travail accélérés CRISPR, vous pouvez obtenir l’ensemble des modifications génétiques bénéfiques parmi des centaines de milliers de gènes knockout.
Les systèmes CRISPR permettent également d’enrichir ou d’épuiser la même souche bactérienne en fonction des besoins spécifiques de la recherche. Par exemple, des chercheurs d’Infinome ont mis en œuvre CRISPR pour concevoir des souches d’E. coli afin d’augmenter la production de lysine, un acide aminé essentiel utilisé comme additif alimentaire. D’autre part, SNIPR a utilisé le même système pour éradiquer les souches d’E. coli néfastes de l’intestin des patients atteints d’un cancer hématologique afin de prévenir les infections de la circulation sanguine.
Prévoir l’avenir de CRISPR
Comme indiqué précédemment, CRISPR favorise la lutte contre les bactéries pathogènes. Il a été prouvé à plusieurs reprises que les traitements antibiotiques traditionnels perturbent le microbiote intestinal en ciblant les bactéries nocives et bénéfiques. CRISPR peut aider à améliorer la spécificité des bactéries pour maintenir l’équilibre du microbiote intestinal humain.
CRISPR est un autre potentiel prometteur : la capacité à concevoir des souches bactériennes avec un potentiel thérapeutique. Il peut être utilisé pour ajouter des fonctions génétiques au microbiome par le biais de bactéries modifiées, qui peuvent exprimer une enzyme ou un métabolite spécifique dont l’organisme manquait auparavant.
Enfin, la mise en œuvre réussie de CRISPR en ingénierie biomédicale et bioindustrielle repose sur la capacité à effectuer des modifications combinatoires, également appelées « remaniement de l’ADN ». En particulier dans les grands systèmes microbiens, la possibilité d’introduire plusieurs modifications pour réduire le nombre de séries de criblage sera primordiale pour mettre en œuvre la production bioindustrielle.
Molecular Devices aide les chercheurs en fournissant des technologies de pointe qui accélèrent l’objectif immédiat de l’édition génomique CRISPR-Cas9. Un criblage précis de la bibliothèque et la sélection des tubes modifiés par CRISPR sont essentiels dans les flux de travail d’ingénierie du microbiome, permettant une disponibilité plus rapide du produit de biofabrication sur le marché.
- Doudna, Jennifer A. et Emmanuelle Charpentier. « La nouvelle frontière de l’ingénierie génomique avec CRISPR-Cas9. » Science 346,6213 ( 2014) : 1258096.
CRISPR在微生物组工程科学突破中的作用
CRISPR首次在海洋细菌的基因组中发现,当面临病毒威胁时,细菌细胞通过捕获和复制病毒的DNA片段来产生免疫反应,这使得细菌能够识别随后的攻击并切割病毒DNA以阻止病毒感染。另外,还发现Cas酶负责切割DNA,这种防御机制后来被Doudna和Charpentier利用,他们可以靶向目标DNA序列,并使用CRISPR-Cas9系统将其分离(1)。
在过去的十年中,CRISPR-Cas9已被证明在药物发现和药物制造中具有巨大的价值。使用合成向导RNA(gRNA),科学家可以靶向目标DNA序列并使用Cas9进行切割。随后,宿主修复机制试图通过非同源末端连接(NHEJ)修复DNA,导致改变基因功能的随机突变。利用这种机制,科学家们现在可以使基因沉默来阐明它们在疾病表型中的作用,这有利于发现目标。此外,科学家还可以利用CRISPR-Cas9,通过识别与免疫系统逃避相关的一组基因来揭示耐药机制。
然而,今天,我们将探索CRISPR的不同应用:微生物组工程。本期内容我们来讨论CRISPR在微生物组工程中的应用以及它如何克服人类微生物组研究的瓶颈。
本次嘉宾:Jakob Haaber博士,副总裁兼交付技术主管SNIPR Biome和Infinome Biosciences联合创始人、CEO 兼CTO Richard Fox博士一起探讨CRISPR的广泛用途,包括治疗和生物制造。
CRISPR-Cas9如何帮助探索人类微生物组在疾病中的作用
众所周知,人体含有数万亿种微生物,在数量上超过了人体细胞。这些微生物统称为微生物组,通过调节细胞外环境和保护细胞免受病原体侵害,与人体形成共生关系。因此,从糖尿病、肥胖到癌症,微生物组的破坏与许多疾病密切相关也就不足为奇了。

通过设计CRISPR-Cas9系统来切割特定的细菌DNA序列以消除致病细菌,这种特异性使CRISPR技术减轻对整体微生物组的破坏,实现药物发现进程的加速。。SNIPR Biome是积极致力于实现这一目标的公司之一,SNIPR Biome副总裁兼CRISPR负责人和交付技术主管Jakob Haaber博士描述了CRISPR在致病性大肠杆菌消除中的应用:“我们使用CRISPR杀死大肠杆菌。目前,治疗细菌感染最常用的就是抗生素。但抗生素耐药性的发生率增加,进而使抗生素无效。CRISPR的优点是它不区分抗生素敏感和抗生素耐药细菌。他还建议,CRISPR可以专门针对致病细菌,而不影响健康肠道微生物组中不可或缺的有益细菌,而不是像抗生素一样,对健康细菌和病原体都有影响。
CRISPR的优势和近年发展

Infinome Biosciences的联合创始人、CEO兼CTO Richard Fox表示,CRISPR的主要优势在于其扩大基因组编辑的能力。“我们现在可以精确地编辑整个通路或基因组,而不是一小部分目标基因上的随机突变,从而引入数十万个变化。
大规模的基因组编辑产生可商用的细胞库,研究人员可以将其整合到高通量表型筛选中。这些库消除了手动敲除大量基因进行表型分析的需要,并为加速药物发现研究提出了解决方案。
CRISPR技术的另一个优点是提高了特异性,微生物组基因编辑是受益于特异性的领域之一。CRISPR系统可以被编程为切割特定的细菌DNA,甚至在不杀死细胞的情况下去除细菌细胞壁内的基因回路。综上所述,这些进步推动了肠道微生物群偏差的新基因疗法。
与此同时,CRISPR系统已经能够制造出更小的基因构建体,以便更容易地装配到递送载体中。因此,除了CRISPR之外,递送载体还可以携带多种成分,构成一种多功能的基于基因的疗法,不仅仅是切割或插入DNA。
加速CRISPR技术的制造
合成生物学和生物工程之间的差距通常是由时间和成本问题引起的。将生物制造解决方案推向市场需要大型实体,这些实体具有完善的基础设施、强大的自动化、大量的人员、仪器、信息学和大量资金。因此,生物制剂的开发可能需要5-10年和数百万美元也就不足为奇了。这是一项风险相当大的投资,因此制药公司往往不愿参与其中,从而一些具有巨大治疗潜力的领域未得到开发。
支持CRISPR的基因组编辑系统的设置是工作流程的瓶颈之一。大规模基因组工程系统的设计非常费力,因为需要产生微量的供体序列来靶向并精确地将10,000个位点编辑到整个基因组。
Infinome Biosciences的联合创始人之一Andrew Garst提出了一项关键创新,将指导切割的引导序列与介导修复的供体序列配对,从而将广基因组编辑减少到只需点击几下。Richard Fox认为,“这种自动化设计和构建系统可以在不到一周的时间内创建编辑过的细胞库,这是过去所花费的努力的一小部分”。
微生物基因编辑步骤
肠道微生物组基因编辑的第一步是CRISPR系统的体外验证。CRISPR编辑的特异性是针对一组代表肠道微生物组的细菌进行测试的,以确保CRISPR系统针对预定的细菌亚种,并且使得有益细菌不受CRISPR诱导的基因编辑的影响。
然后,验证继续进行到临床前和临床研究。利用基因组测序技术,研究人员证明基因编辑不会以有害的方式扰乱微生物组。当然,脱靶效应不可避免地会发生,正如全基因组测序所揭示的那样。我们需要做是监测发生率,并确保这些影响是微不足道的,不会干扰基因编辑。
测序和表型分析揭示了基因组携带的一组编辑以及细菌种群中的主要菌株。为了进一步验证靶向基因组编辑的成功,可以将细菌种群置于环境压力源中并监测其行为。这确保了基因编辑赋予细菌所需的特性,例如在缺氧等环境压力下生长的能力。

通过加速的CRISPR工作流程,研究人员可以在数十万个基因敲除中得到一组有益的基因编辑。
CRISPR系统还可以根据特定的研究需求,灵活地富集或消耗相同的细菌菌株。例如,Infinome的研究人员应用CRISPR来设计大肠杆菌菌株,以扩大赖氨酸的生产,赖氨酸是一种用作食品添加剂的关键氨基酸。另一方面,SNIPR使用相同的系统从血液癌患者的肠道中根除有害的大肠杆菌菌株,以防止血液感染。
展望
如前所述,CRISPR能够对抗致病菌,已多次证明,传统的抗生素治疗通过作用有害和有益细菌来破坏肠道微生物群。CRISPR可以帮助增强细菌的特异性,以维持人类肠道微生物群的平衡。
另一个令人兴奋的前景是设计具有治疗潜力的细菌菌株的能力。这可用于通过工程细菌为微生物组添加遗传功能,这些细菌可以表达身体以前缺乏的特定酶或代谢物。
最后,CRISPR在生物医学和生物工业工程中的成功应用依赖于进行组合编辑的能力,也称为“DNA洗牌”。特别是在大型微生物系统中,引入多次编辑以减少筛选轮次的能力对于生物工业生产至关重要。
Molecular Devices通过提供前沿技术来帮助科学家加速CRISPR-Cas9基因组编辑的近期目标。准确的文库筛选和CRISPR编辑命中物的选择是微生物组工程工作流程的关键,使生物制造产品更快地推向市场。
1. Doudna, Jennifer A.和Emmanuelle Charpentier。“CRISPR-Cas9基因组工程的新前沿。科学346,6213(2014):1258096。