
Organoïdes de cancer colorectal (CCR)
Organoïdes de cancer colorectal dérivés de patients
Les organoïdes dérivés de patients (PDO) pour le cancer colorectal sont des modèles de culture cellulaire tridimensionnels (3D) qui reproduisent la physiologie épithéliale de l’intestin et les caractéristiques génétiques du patient atteint de CRC. Ces PDO CRC modélisent les interactions entre les cellules et l’afflux d’oxygène et de nutriments dans le micro-environnement tumoral. Lorsqu’ils sont cultivés en laboratoire, ces organoïdes tumoraux servent de mini répliques multicellulaires de la tumeur en 3D et ont démontré leur capacité à conserver ses caractéristiques in vivo.
Les organoïdes CRC (et ceux d’autres organes du corps) sont dérivés de cellules souches d’adultes isolées à partir de biopsies de patients. Le tissu est traité en laboratoire et intégré dans une matrice de membrane basale gélatineuse qui apporte un support physique et des facteurs de croissance. Les cellules souches du tissu se divisent pour former plusieurs types de cellules (y compris davantage de cellules souches) qui s’auto-assemblent en structures tridimensionnelles imitant la conformation architecturale et la physiologie de la tumeur d’origine. Une fois formées, ces structures peuvent être séparées pour re-ensemencer plusieurs nouveaux PDO qui s’auto-assemblent de la même manière. De cette façon, le nombre d’organoïdes peut être élargi pour en fournir beaucoup plus, selon les besoins.
Avantages des organoïdes de cancer colorectal dérivés de patients
La représentation des altérations génétiques et de la composition tumorale associées au CRC rend les PDO CRC idéaux pour la recherche sur le cancer et la découverte de médicaments. Les PDO CRC biologiquement pertinents peuvent présenter des réponses médicamenteuses similaires à celles des patients, illustrant leur valeur dans la prédiction de l’efficacité de nouveaux agents thérapeutiques. Cependant, les flux de travail traditionnels de tests manuels d’organoïdes ne se prêtent pas au criblage de composés reproductible haut débit pour la découverte de médicaments.
Les avancées en matière d’extrapolation des organoïdes et d’automatisation des tests ont permis de normaliser les flux de travail PDO CRC. Nos organoïdes 3D Ready sont fabriqués dans un environnement industriel à l’aide de notre technologie de bioréacteur exclusive et de procédés rigoureusement contrôlés. Plusieurs millions d’organoïdes standardisés, de tailles constantes et testés pour la qualité peuvent maintenant être générés en un seul lot. Les organoïdes de CCR peuvent être cryoconservés et utilisés lorsque cela est nécessaire pour des tests haut débit. L’utilisation de la manipulation de liquides pour étaler les PDO dans des boîtes multi-puits et traiter avec des composés réduit significativement les erreurs et le temps de manipulation. Les changements liés au traitement médicamenteux peuvent être évalués à l’aide de tests et d’analyses d’images adaptés.
Flux de travail de culture et de test de tumoroïdes de cancer colorectal
L’évaluation des effets des médicaments sur les tumoroïdes colorectaux peut être automatisée. Le flux de travail ci-dessous décrit l’évaluation automatisée des effets des composés anticancéreux. L’extrapolation des PDO est obtenue grâce à l’expansion dans un bioprocédé utilisant la technologie des bioréacteurs. Après avoir traité les organoïdes avec l’agent à tester, l’analyse morphologique est réalisée par le système d’imagerie à haut contenu ImageXpress® Micro Confocal, tandis que le lecteur de microplaques multimode SpectraMax® iD5 est utilisé pour le test de viabilité. Le flux de travail comprend l’incubation automatisée et la manipulation des liquides, ainsi qu’un logiciel de programmation pour le transfert des plaques de l’incubateur au manipulateur de liquides et au lecteur de plaques.

Protocole expérimental pour les PDO CRC
- Bioprocédé des organoïdes - L’expansion des PDO CRC s’effectue manuellement et ils sont ensemencés dans des bioréacteurs. Les organoïdes qui en résultent sont comptés et évalués afin de déterminer leur plage de tailles finale. Un nombre défini d’organoïdes sont placés dans des flacons et cryoconservés afin d’être prêts à l’emploi à la convenance de l’utilisateur.
- Décongélation - Les PDO sont décongelés à 37 °C, lavés avec du milieu frais et granulés.
- Semence - Les PDO sont en suspension dans la matrice de membrane en hydrogel ou basale requise pour l’ensemencement de plaques multi-puits à la densité requise.
- Traitement - 48 heures après l’ensemencement, les composés ou agents à tester peuvent être ajoutés aux PDO dans les puits aux concentrations requises.
- Imagerie et analyse - L’imagerie par lumière transmise (LT) est réalisée cinq jours après le traitement du composé pour déterminer les paramètres souhaités tels que le nombre d’organoïdes, le diamètre moyen, le volume moyen, la surface totale couverte par les organoïdes, la morphologie, etc.
- Test de viabilité – Exemple de protocole de test de point final
- Réactif de test de viabilité - Un manipulateur de liquide automatisé est utilisé pour ajouter le réactif de test aux puits pour un test de viabilité cellulaire ATP luminescent, tandis que l’agitation automatisée de la microplaque sert de médiateur à la lyse cellulaire.
- Incubation - L’incubation est réalisée à température ambiante pendant 25 minutes.
- Test de viabilité cellulaire ATP luminescent - Le logiciel de programmation et un manipulateur d’échantillons sont utilisés pour transférer la microplaque de l’incubateur au manipulateur de liquides et au lecteur de microplaques. Les résultats sont analysés avec un logiciel de contrôle de lecteur de microplaques et d’analyse de données.
Nous fournissons des solutions d’automatisation de laboratoire complètes pour les flux de travail personnalisés des organoïdes colorectaux. Chaque étape, de la culture et de l’ensemencement des organoïdes, à la manipulation de liquides et à l’acquisition d’images, peut être automatisée et associée à nos solutions logicielles d’analyse de données pour générer des rapports conformes aux réglementations et prêts à être publiés sur vos tests d’organoïdes.
Atout présenté
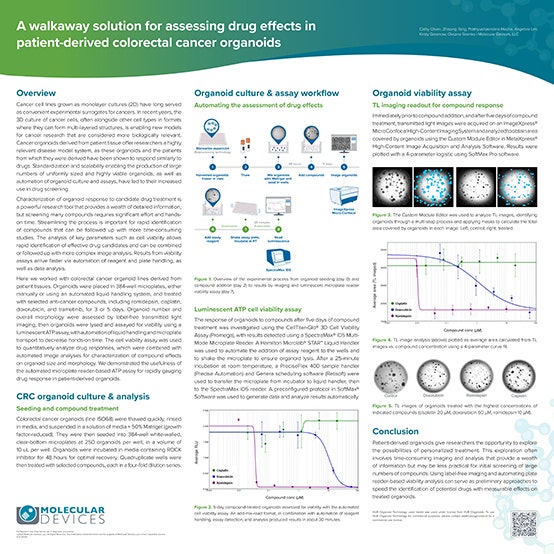
Une solution sans surveillance pour évaluer les effets des médicaments dans les organoïdes de cancer colorectal dérivés de patients
Sur cette affiche scientifique, des organoïdes de cancer colorectal dérivés de patients ont été mis en culture et traités avec des composés anticancéreux tels que la romidepsine, le cisplatine, la doxorubicine et le tramétinib.
L’imagerie par lumière transmise sans marquage (label-free) a révélé des variations dépendantes du nombre d’organoïdes et de la surface totale occupée par les organoïdes en réponse au traitement médicamenteux. Un test ATP luminescent sur lecteur de plaques a permis de recueillir les données quantitatives de viabilité cellulaire à partir des organoïdes.
Le flux de travail implique une manipulation automatisée des liquides, un transfert sur microplaques et des méthodes d’analyse logicielle pour réduire le temps de manipulation et accélérer le criblage des médicaments.
Dernières ressources
La complexité des structures des organoïdes colorectaux nécessite des stratégies avancées d’imagerie et d’analyse. De plus, les étapes fastidieuses et laborieuses doivent être automatisées pour un délai d’exécution plus rapide et une homogénéité accrue. Découvrez comment l’analyse qualitative et quantitative haut débit des tumoroïdes peut être réalisée grâce à des stratégies d’automatisation.