
Évolution du rôle des cellules CHO dans le développement de lignées cellulaires
Depuis la première approbation de l’insuline recombinante et de l’hormone de croissance humaine au début des années 1980, une multitude de protéines thérapeutiques recombinantes ont été approuvées par les organismes de réglementation, notamment la FDA aux États-Unis et l’EMA en Europe. Compte tenu de cette augmentation significative de l’introduction réussie d’agents thérapeutiques biologiques, il existe un besoin crucial dans l’espace de découverte de médicaments pour soutenir des processus de fabrication plus efficaces qui nécessitent des lignées cellulaires hautement productives.
Les cellules ovariennes de hamster chinois (CHO) sont des lignées cellulaires semblables à des cellules épithéliales qui sont très sensibles à la transfection et sont devenues la référence pour la fabrication de protéines thérapeutiques approuvées.
Pourquoi les cellules CHO sont-elles utilisées ?
Plusieurs propriétés clés des cellules CHO ont conduit à leur établissement en tant que lignée cellulaire hôte préférée pour les approbations réglementaires des produits thérapeutiques recombinants :
1
Adaptable à la croissance de la culture en suspension, ce qui est idéal pour la production à grande échelle dans les bioréacteurs
2
Adaptable à la croissance dans des milieux de culture sans sérum et chimiquement définis (sans animaux), ce qui garantit la reproductibilité entre les différents lots de culture cellulaire
3
Permettre des modifications post-traductionnelles (par ex. glycosylations) des protéines recombinantes qui sont compatibles et bioactives chez l’homme
4
Plusieurs systèmes de sélection chimique et d’amplification génétique ont été développés pour les cellules CHO, optimisés pour un rendement plus élevé de protéine recombinante par cellule.
Historique des cellules CHO
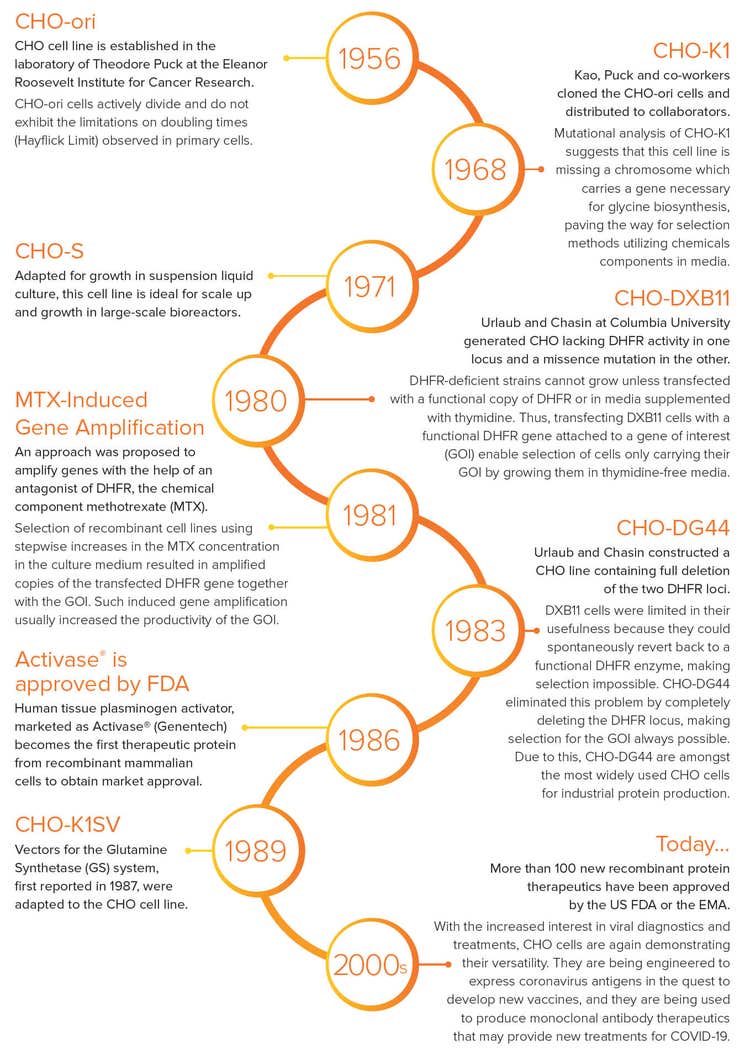
1956 -Cellules CHO-ori
La lignée cellulaire CHO est établie dans le laboratoire de Theodore Puck à l’Eleanor Roosevelt Institute for Cancer Research. Les cellules CHO-ori se divisent activement et ne présentent pas les limitations des temps de doublement (limite de Hayflick) observées dans les cellules primaires.
1968 -Cellules CHO-K1
Kao, Puck et leurs collègues ont cloné les cellules CHO-ori et les ont distribuées aux collaborateurs. L’analyse mutationnelle de CHO-K1 suggère qu’il manque à cette lignée cellulaire un chromosome qui porte un gène nécessaire à la biosynthèse de la glycine, ouvrant la voie à des méthodes de sélection utilisant des produits chimiques CHO-S dans le milieu.
1971 -Cellules CHO-S
Adaptée à la croissance dans des cultures liquides en suspension, cette lignée cellulaire est idéale pour la mise à l’échelle et la croissance dans des bioréacteurs à grande échelle.
1980 -Cellules CHO-DXB11
Urlaub et Chasin de l’Université de Columbia ont généré un CHO dépourvu d’activité DHFR dans un locus et une mutation de missence dans l’autre. Les souches déficientes en DHFR ne peuvent pas se développer à moins d’être transfectées avec une copie fonctionnelle de DHFR ou dans un milieu supplémenté en thymidine. Ainsi, la transfection de cellules DXB11 avec un gène DHFR fonctionnel attaché à un gène d’intérêt (GOI) permet de sélectionner des cellules portant uniquement leur GOI en les développant dans un milieu sans thymidine.
1981 -Amplification génique induite par le MTX
Une approche a été proposée pour amplifier les gènes avec l’aide d’un antagoniste du DHFR, le composant chimique méthotrexate (MTX). La sélection de lignées cellulaires recombinantes en utilisant des augmentations progressives de la concentration de MTX dans le milieu de culture a donné lieu à des copies amplifiées du gène DHFR transfecté avec le GOI. Une telle amplification génétique induite augmente généralement la productivité du GOI.
1983 -Cellules CHO-DG44
Urlaub et Chasin ont construit une ligne CHO contenant la suppression complète des deux loci DHFR. L’utilité des cellules DXB11 était limitée, car elles pouvaient spontanément revenir à une enzyme DHFR fonctionnelle, ce qui rendait leur sélection impossible. CHO-DG44 a éliminé ce problème en supprimant complètement le locus DHFR, ce qui rend toujours possible la sélection du GOI. Pour cette raison, CHO-DG44 est l’une des cellules CHO les plus largement utilisées pour la production de protéines industrielles.
1986 -Activase® est approuvé par la FDA
L’activateur du plasminogène tissulaire humain, commercialisé sous le nom d’Activase® (Genentech) devient la première protéine thérapeutique des cellules de mammifères recombinantes à obtenir l’approbation de mise sur le marché.
1989 -Cellules CHO-K1SV
Les vecteurs pour le système de synthétase de glutamine (GS), rapportés pour la première fois en 1987, ont été adaptés à la lignée cellulaire CHO.
2000 -Aujourd’hui...
Plus de 100 nouvelles protéines thérapeutiques recombinantes ont été approuvées par la FDA américaine ou l’EMA.
Avec l’intérêt croissant pour les diagnostics et les traitements viraux, les cellules CHO démontrent à nouveau leur polyvalence. Ils sont conçus pour exprimer les antigènes du coronavirus dans la quête de nouveaux vaccins, et ils sont utilisés pour produire des anticorps monoclonaux thérapeutiques qui peuvent fournir de nouveaux traitements contre la COVID-19.
Générer des cellules CHO recombinantes
Découvrez un processus efficace et rapide pour générer des lignées cellulaires CHO recombinantes
La sélection de lignées cellulaires CHO de mammifères à production élevée continue de représenter un goulot d’étranglement majeur dans le développement de procédés pour la production de produits biopharmaceutiques. Par conséquent, il est de plus en plus important de développer de nouvelles méthodes haut débit pour la sélection de lignées cellulaires CHO à expression élevée de manière efficace et rentable.
Dans cette note d’application, découvrez un processus efficace et rapide pour générer des lignées cellulaires CHO recombinantes, produisant des niveaux élevés de protéines thérapeutiques.
Télécharger la note d’application

Molecular Devices offre une solution rapide, simple et complète pour le développement de lignées cellulaires CHO . Associés à l’agent de détection CloneDetect, CloneSelect™ Imager et au système ClonePix™ , ils permettent aux chercheurs de développer plus efficacement de nouvelles lignées cellulaires CHO productrices de protéines et d'accélérer ainsi la mise sur le marché.