Organoïdes
La recherche biologique et la modélisation de maladies résument la complexité des tissus réels
Que sont les organoïdes ?
Les organoïdes sont des micro-tissus multicellulaires en trois dimensions (3D) dérivés de cellules souches et conçus pour imiter fidèlement la structure et la fonctionnalité complexes des organes humains comme le poumon, le foie ou le cerveau. Les organoïdes sont multi-cellulaires et présentent un ordre supérieur d’auto-assemblage permettant une représentation encore meilleure des interactions et des réponses cellulaires in vivo complexes par rapport aux cultures cellulaires traditionnelles en 2D.
Un organoïde peut être défini de trois façons différentes :
- Il s’agit d’un micro-tissu biologique 3D contenant plusieurs types de cellules
- Il représente la complexité, l’organisation et la structure d’un tissu
- Et, sous certains aspects, il possède la fonctionnalité d’untissu
Les organoïdes sont de plus en plus importants dans les domaines de la recherche sur le cancer, la neurobiologie, la recherche sur les cellules souches et la découverte de médicaments, car ils permettent une meilleure modélisation des tissus humains. Dérivés de cellules souches, les organoïdes peuvent être différenciés en une vaste gamme de types de tissus, notamment le foie, le poumon, le cerveau, le rein, l’estomac et l’intestin. Comme ces micro-tissus 3D imitent les organes in vivo, ils peuvent vous fournir davantage d’informations sur les mécanismes du développement humain et les maladies. Par exemple, vous pouvez développer des organoïdes à partir de cellules génétiquement modifiées afin de comprendre comment des mutations génétiques spécifiques sont associées à certains troubles génétiques. Les organoïdes peuvent également faciliter l’étude des maladies infectieuses et des interactions hôte-agent pathogène. Enfin, la capacité d’utiliser des organoïdes dérivés de patients pour le criblage de médicaments et les évaluations de la toxicité permet aux chercheurs de faire des avancées en médecine personnalisée.
Flux de travail général concernant la culture et le criblage des organoïdes
En raison de la complexité croissante des organoïdes et d'autres systèmes cellulaires 3D, des techniques d’imagerie 3D et d’analyse plus sophistiquées sont nécessaires afin de caractériser ces tests biologiques de façon précise et efficace. Actuellement, les systèmes d’imagerie confocale automatisés et les logiciels d’analyse d’images 3D sont couramment utilisés pour aider les chercheurs à simplifier leur flux de travail et à obtenir des résultats optimaux.
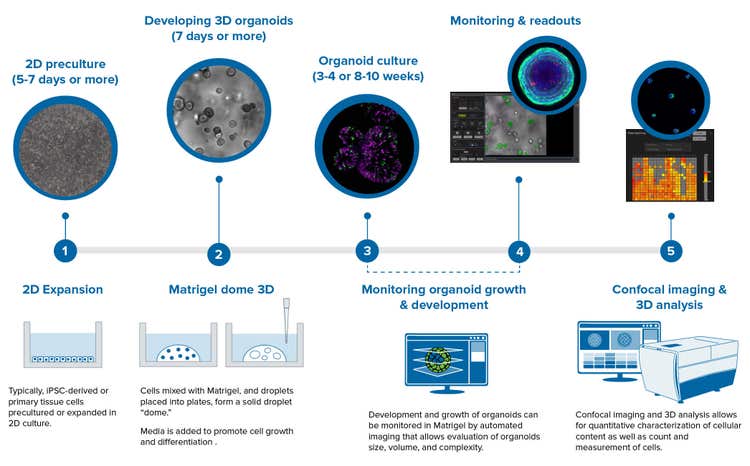
Étape 1) Préculture 2D
Les organoïdes dérivent soit de cellules primaires (par exemple, intestin, poumon ou rein) soit de cellules souches pluripotentes induites. Les cellules souches sont capables de se différencier et de s’auto-assembler en divers organoïdes spécifiques aux tissus.
Étape 2) Développement d’organoïdes 3D
Généralement, les cellules sont prémélangées avec du Matrigel et des gouttelettes sont placées dans une plaque de 24 puits à la température ambiante. Les plaques sont ensuite placées dans un incubateur afin de former un dôme solide de gouttelettes. Du milieu est alors ajouté pendant au moins 7 jours afin de favoriser la croissance et la différenciation des cellules dans un tissu spécifique (cerveau, intestin, poumons, etc.). Le milieu inclut des protéines de la matrice extracellulaire (MEC) et différents facteurs de croissance, qui varient selon le type de tissu à faire croître.
Étape 3) Culture d’organoïdes
La culture d’organoïdes est un long processus pouvant comprendre plusieurs étapes utilisant des milieux différents. Durant ce processus, la santé cellulaire doit être surveillée (par imagerie), ce qui est généralement utilisé pour comprendre la biologie développementale et les tissus.
Étape 4) Surveillance et résultats
Avant de réaliser des expériences, les organoïdes doivent être surveillés et caractérisés afin de s’assurer qu’ils ont la structure et la différenciation tissulaires appropriées. L’imagerie haut contenu permet la surveillance et la visualisation de la croissance et de la différenciation des organoïdes, la reconstruction 3D des structures, l’analyse complexe de la structure des organoïdes, la morphologie et la viabilité cellulaires, ainsi que l’expression de différents marqueurs cellulaires.
Étape 5) Imagerie confocale et analyse 3D
L’imagerie confocale et l’analyse 3D des organoïdes permettent de visualiser et de quantifier les organoïdes et les cellules qui les composent. La caractérisation de multiples descripteurs quantitatifs des organoïdes pourrait être utilisée pour étudier les phénotypes des maladies et les effets des composés.
Imagerie confocale et analyse d’images 3D des organoïdes
Les organoïdes sont très utiles pour la modélisation des maladies et l’évaluation des effets des composés. L’imagerie et l’analyse automatisées des organoïdes sont importantes pour l’évaluation quantitative des variations phénotypiques dans les organoïdes, ainsi que pour l’augmentation du débit des expérimentations et des criblages.
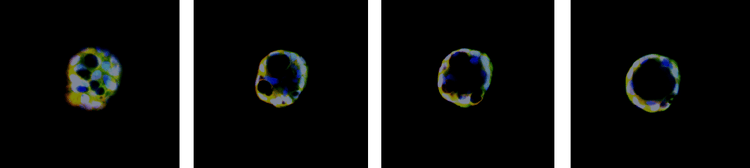
L’imagerie confocale, comme le système ImageXpress® Confocal HT.ai avec des lasers haute performance et des objectifs à immersion dans l’eau, sont particulièrement utiles pour capturer la complexité des tests biologiques 3D. Contrairement aux sphéroïdes habituels, qui ont l’apparence d’objets solides et pour lesquels la pénétration de la lumière est limitée, certains organoïdes 3D, tels que les organoïdes pulmonaires, ont une apparence creuse, avec une lumière ou des cavités à l’intérieur, et sont plus facilement pénétrés par la lumière, ce qui permet de réaliser une « imagerie traversant » les micro-tissus enchâssés dans du Matrigel.
Les outils d’analyse haut contenu, comme le MetaXpress ou le logiciel d’analyse d’images IN Carta, permettent de trouver et de caractériser de multiples objets/organoïdes, soit au format 2D (pour des images sur un plan unique ou pour des images de projection maximales), soit au format 3D lorsque des objets issus de plusieurs plans sont reliés et reconstitués dans un espace 3D par un logiciel. Les organoïdes peuvent être caractérisés en terme de diamètre, de volume, de forme, d’intensité d’un marqueur spécifique ou de la distance par rapport à d’autres objets.
En outre, des cellules, des noyaux ou des organites individuels peuvent être définis et mesurés au sein de chaque organoïde. Cela permet de compter le nombre de cellules vivantes et de cellules mortes, ou le nombre de cellules avec un marqueur spécifique pour définir également les volumes et les distances entre les objets. Les valeurs numériques peuvent être comptées pour chaque organoïde ou pondérées par puits.
Galerie d’images de cellules d'organoïdes pulmonaires
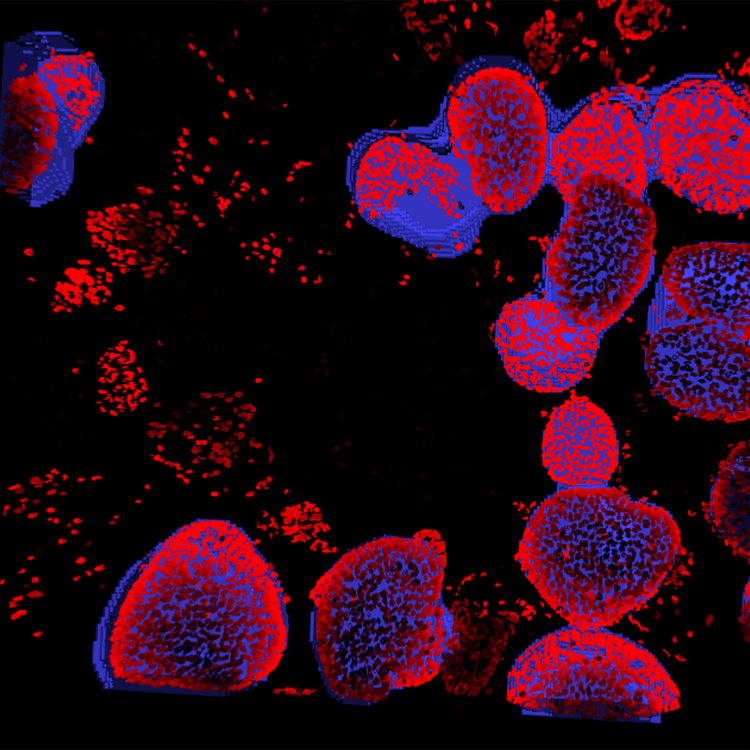
Analyse d’images d’organoïde
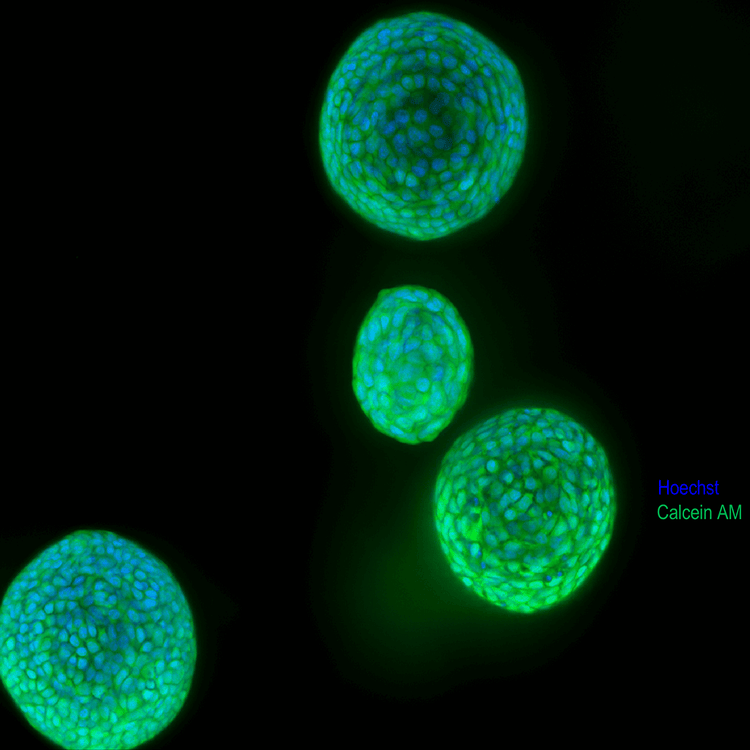
Organoïdes pulmonaires
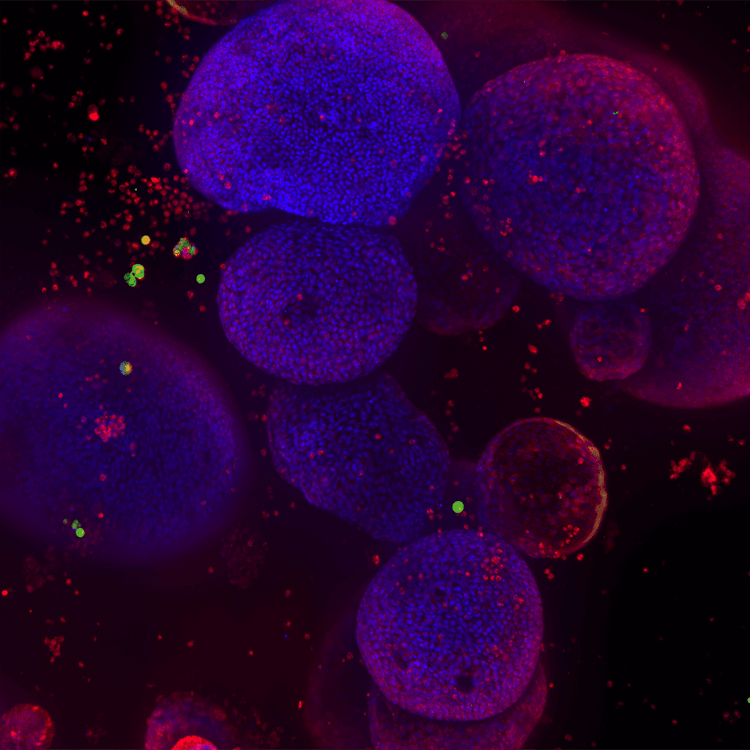
Organoïdes pulmonaires 2

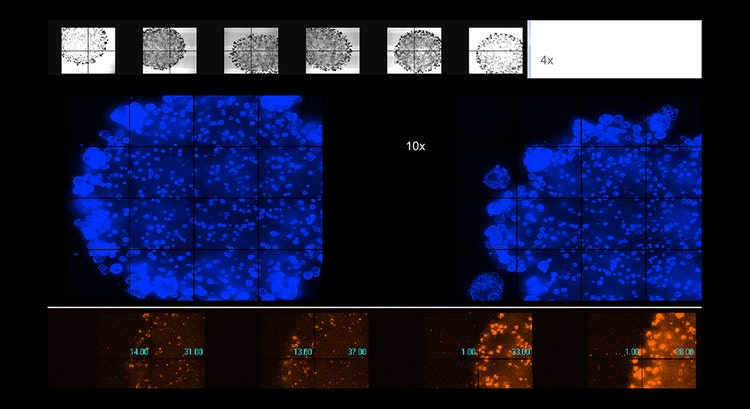
Une imagerie automatisée d’organoïdes vivants dans du Matrigel a été réalisée en utilisant une option confocale, en grossissement 4x ou 10x
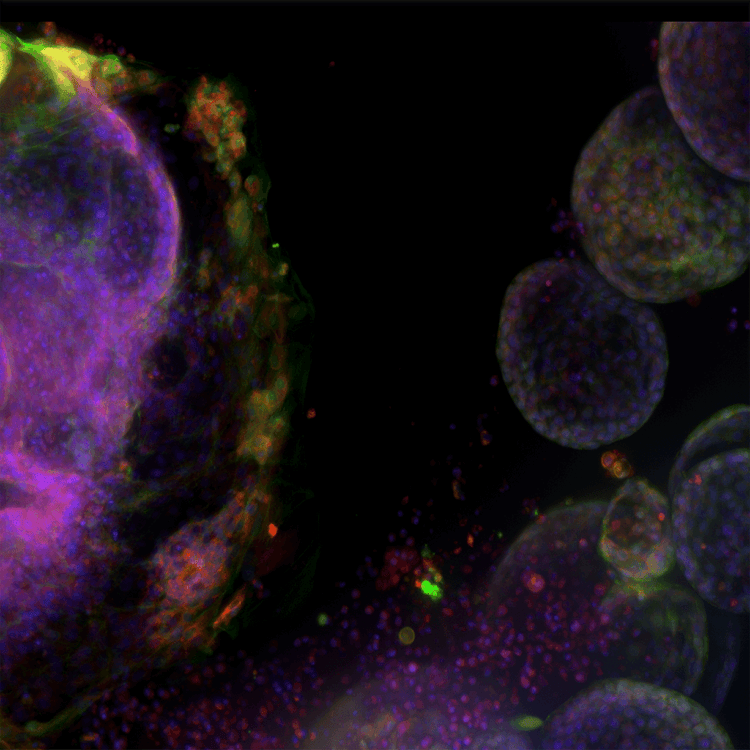
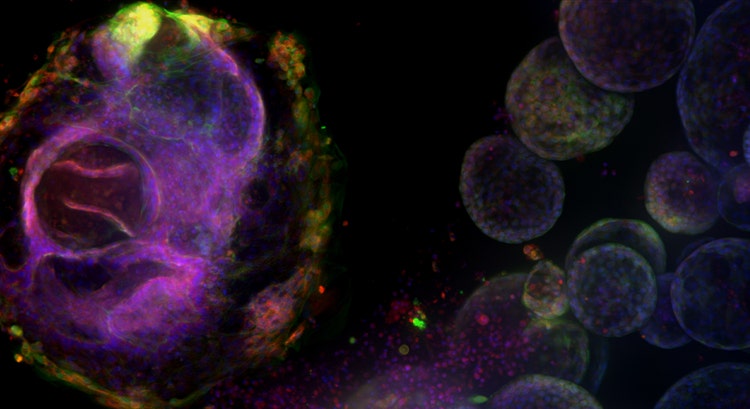
Organoïde pulmonaire hautement complexe
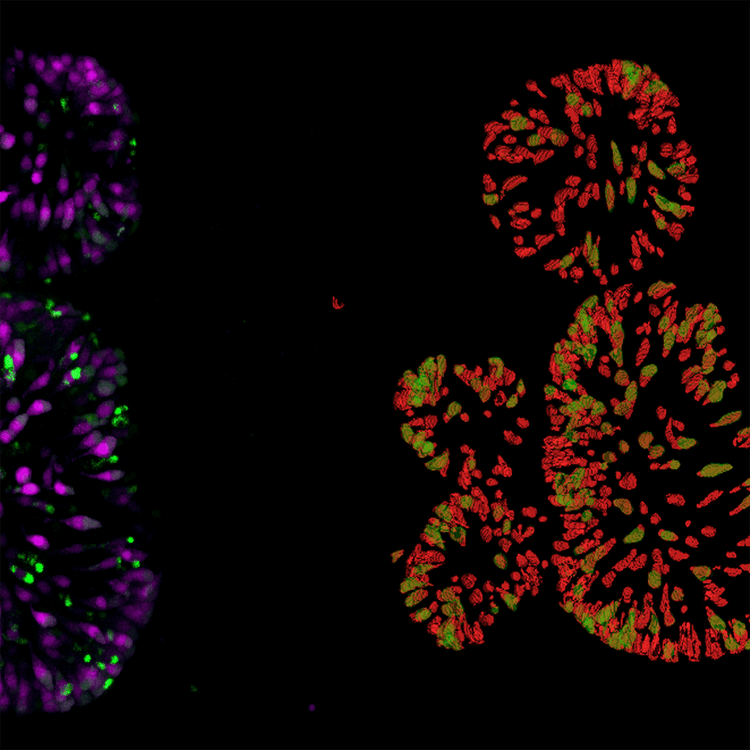
Organoïde intestinal de cellules rouge tomate Détection d’un double positif (mNeon) en vert
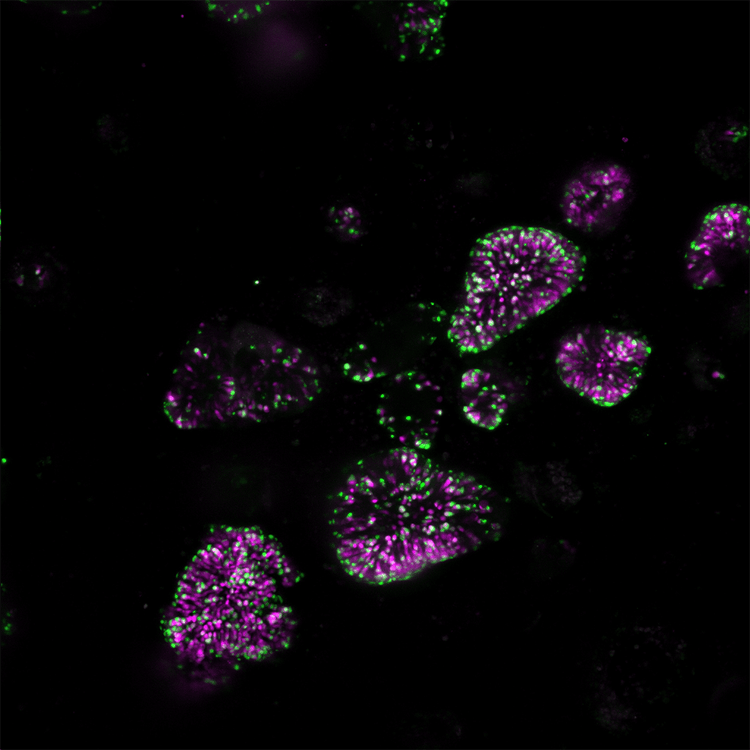
Gènes exprimés au plan interne 10x, dTomato Magenta, mNeon Green
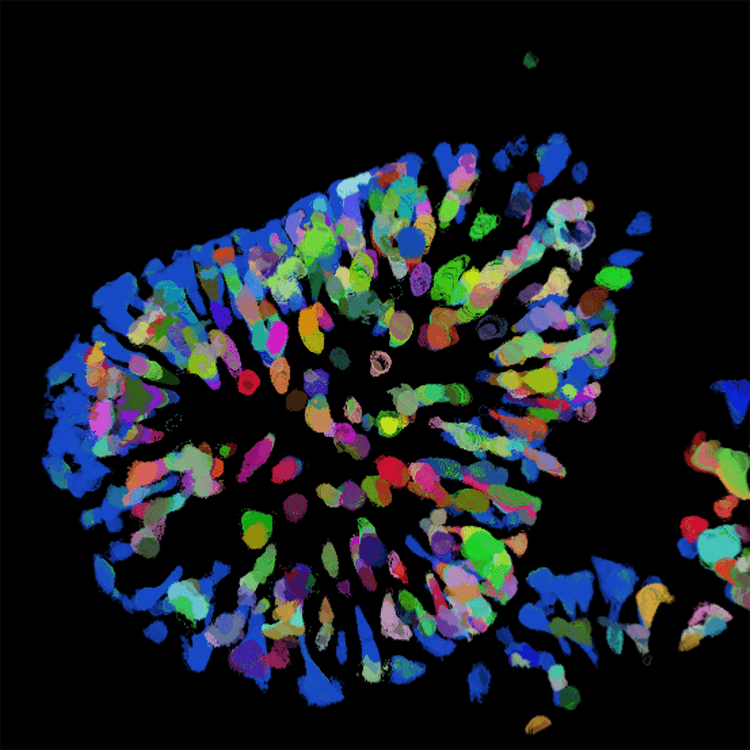
Organoïde intestinal 40x, numération des cellules dTomato Magenta
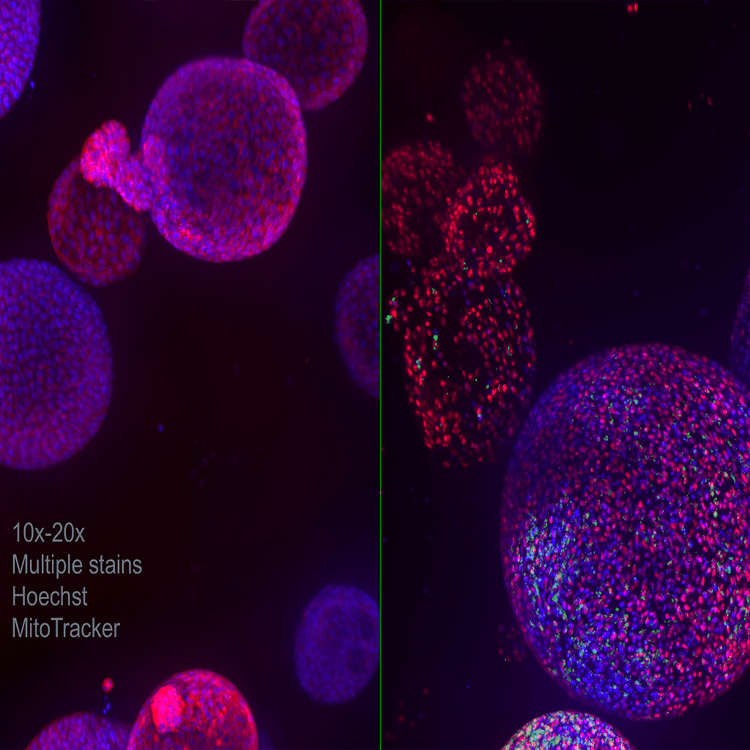
Organoïde pulmonaire 10x 20x Plusieurs souches Hoechst MitoTracker
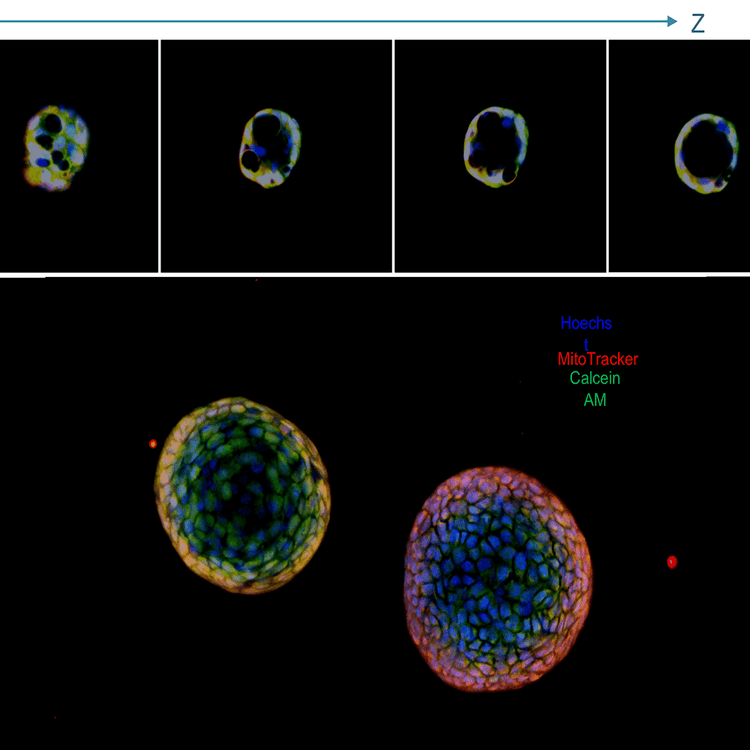
Organoïdes pulmonaires, image de projection et panel avec Z Stack ; cellules vivantes marquées au bleu Hoechst, noyaux), MitoTracker (rouge, mitochondrie) et calcéine AM(vert, colorant de viabilité) ; immersion dans l'eau 20x
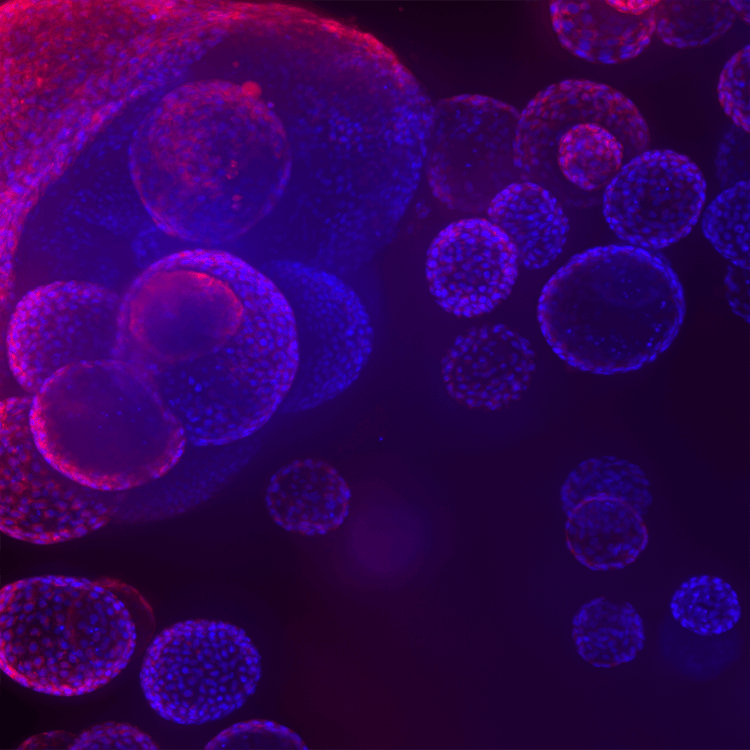
Organoïdes pulmonaires 3
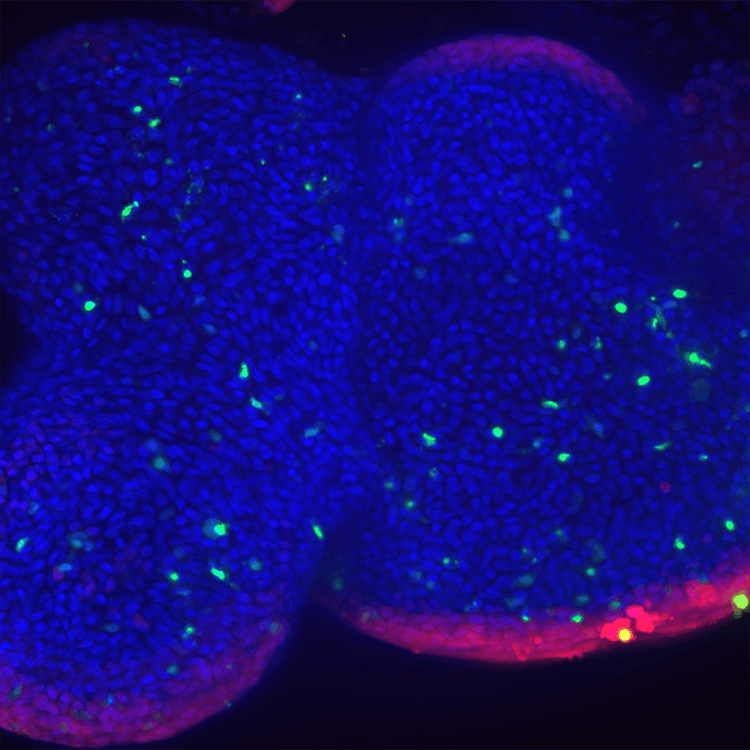
Organoïdes pulmonaires 4
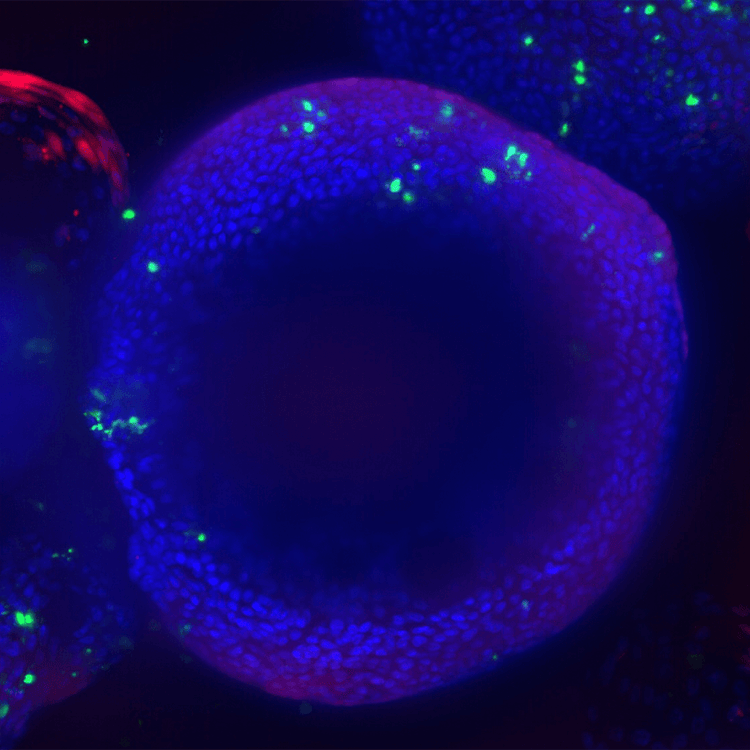
Organoïdes pulmonaires, cellules épithéliales des voies respiratoires mises en culture dans des dômes de Matrigel durant 8 semaines
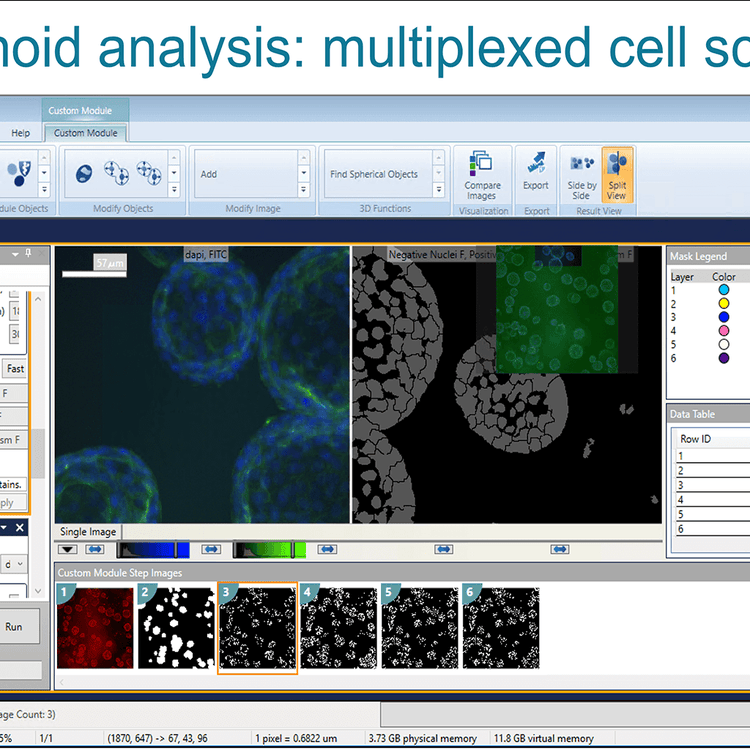
Cell Scoring multiplexé d’analyse d’organoïdes
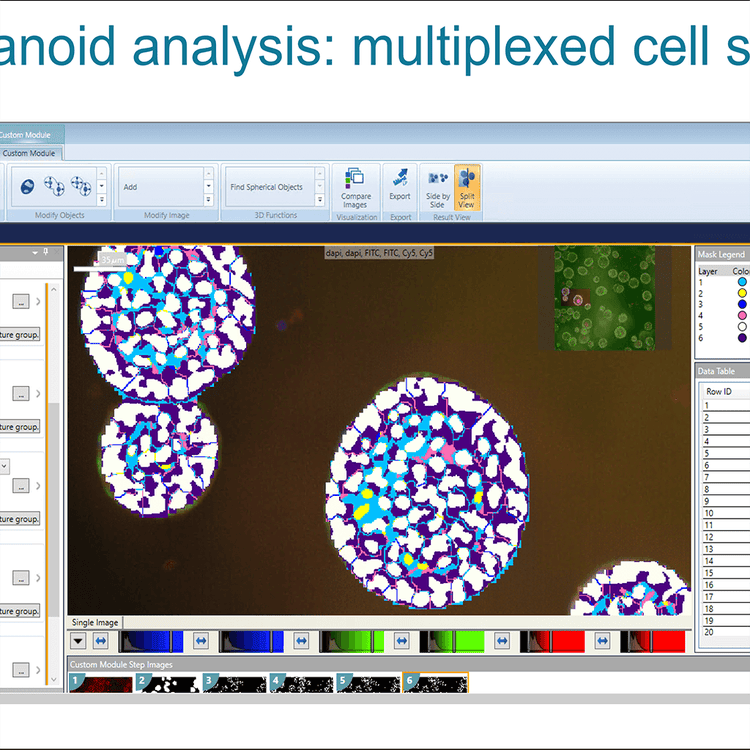
Cell Scoring multiplexé d’analyse d’organoïdes2
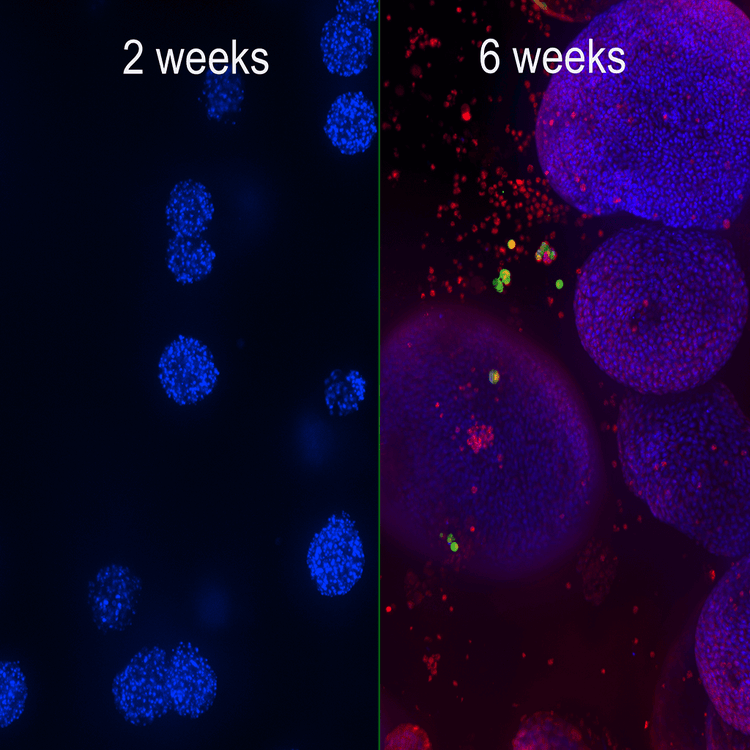
Développement d'organoïdes