
Course contre la montre dans le contexte COVID-19 : Diagnostics, vaccins et développement d’anticorps thérapeutiques
Les efforts mondiaux de la recherche sont axés sur les connaissances sur le virus SARS-CoV-2 afin de développer des traitements potentiels contre la COVID-19. Rejoignez-nous pour découvrir un calendrier scientifique des principales découvertes sur la COVID-19. L’infographie met en avant le développement historique des diagnostics, des vaccins et des anticorps thérapeutiques. Nous partagerons nos solutions de flux de travail pour les défis du diagnostic, du traitement et de la prévention en offrant des systèmes clés pour vous aider à accélérer vos recherches sur la COVID-19 et votre délai de mise sur le marché.
1. Développement de diagnostic : La commercialisation du premier test PCR de dépistage de la COVID
Le virus SARS-CoV-2, l’agent responsable de la COVID-19 et la pire pandémie de l’histoire moderne, a été identifié pour la première fois dans des cas isolés fin 2019. La séquence génétique du virus a été obtenue tôt 2020 et ensuite partagée avec les laboratoires de recherche du monde entier. La course à la compréhension des fondements moléculaires du virus et au développement de traitements et de vaccins efficaces était en cours.

- Janvier 2020 – Le SARS-CoV-2 a été mis en culture en laboratoire pour la première fois à des fins de recherche. Il s’agissait d’une pièce critique du puzzle pour le développement de tests de diagnostic et de vaccins.\
- Février – mars 2020 – De nombreux tests génétiques basés sur PCR, ELISA et d’autres techniques sont apparus pour répondre aux défis de la détermination des cas positifs d’infection virale et de la lutte contre la propagation de la maladie.\
- Avril 2020 – Dix-huit tests développés en laboratoire (LDT) avaient obtenu l’autorisation d’utilisation d’urgence (EUA) de la FDA, un nombre qui doublerait en un mois.\
- Septembre 2020 – Le nombre de tests de diagnostic EUA atteint plus de 250, y compris plus de tests 200 moléculaires, tests d’50anticorps et tests multiples basés sur des antigènes. Ces tests couvraient le cycle de vie de l’infection virale, de la détection précoce du virus dans le cas de tests moléculaires et antigéniques à la mesure des réponses immunitaires par détection d’anticorps hôtes.
Procédé de développement de diagnostic utilisant ELISA
Le processus de développement du diagnostic peut comprendre plusieurs étapes dans l’identification de biomarqueurs indicatifs de virus. Ces signatures incluent**** signatures génétiques dans le cas de la RT-PCR, ou antigènes viraux dans le cas de la détection basée sur antigène. La détection de l’antigène viral et de l’anticorps hôte peut être obtenue en utilisant l’essai immunologique enzymatique (ELISA) et d’autres approches quantitatives. La caractérisation précoce est primordiale pour comprendre les cibles clés pour lesquelles des tests et des tests seront développés.
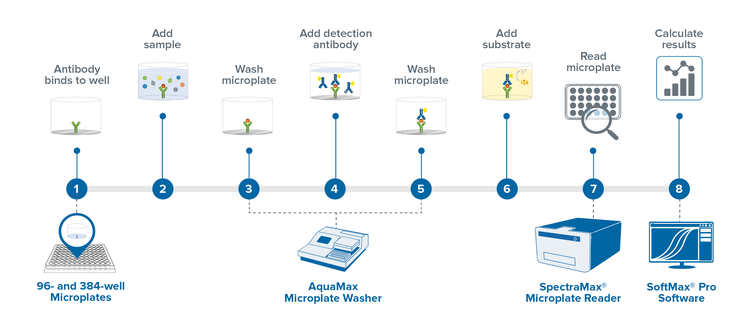
Le flux de travail ci-dessus pour une procédure ELISA sandwich typique est long et laborieux ; une automatisation de laboratoire pour un flux de travail ELISA haut débit peut aider à fournir un temps sans surveillance, à augmenter le débit, l’efficacité et l’efficience de la procédure de test, et la reproductibilité.
Les lecteurs de microplaques en absorbance SpectraMax ABS et ABS Plus offrent flexibilité, sensibilité et facilité de réalisation pour un grand nombre de tests tels que les tests ELISA, la croissance microbienne et la quantification des protéines.
Les lecteurs de microplaques multimode SpectraMax® iD3 et iD5 mesurent l’absorbance, la fluorescence et la luminescence. En outre, le lecteur iD5 mesure la TRF et la FP et peut être élargi pour inclure TR-FRET, HTRF®, BRET, les tests rapporteurs à double luciférase avec injecteurs et la détection Western Blot.
Le lecteur de microplaques multimode SpectraMax® i3x mesure l’absorbance, la fluorescence et la luminescence grâce à des mises à niveau disponibles, notamment le Western Blot, l’imagerie cellulaire et la cinétique rapide avec injecteurs, ainsi que des modes de détection supplémentaires.
Le laveur de microplaques AquaMax® est un système totalement autonome, configurable pour les microplaques à 96 et 384 puits.
2. développement d’un vaccin L’effort mondial pour accélérer les vaccins contre la COVID
Sur un autre front, une campagne massive était menée dans le développement de vaccins pour prévenir l’infection par le SARS-CoV-2 et sa propagation. Sur la base de plusieurs années de travail exploratoire et préclinique, plusieurs entreprises ont exploité la séquence génétique du virus dans la création de nouveaux vaccins à base d’ARNm. D’autres voies de développement de vaccins ont également été explorées, notamment celles basées sur des systèmes d’administration de vecteurs viraux et l’administration plus traditionnelle de particules virales tuées ou atténuées. Une approche à plusieurs volets était essentielle pour déterminer les stratégies de prévention les plus efficaces.

- Avril 2020 – Moderna et Pfizer avaient terminé la recherche préclinique et le développement de vaccins candidats à ARNm. Johnson & Johnson et Astra Zeneca ont mené des essais cliniques sur leurs vaccins candidats au cours des semaines suivantes. Ces efforts ont été les premiers dans une vague de développement de vaccins , avec plus de 80 vaccins candidats en cours de développement et au moins cinq en phase 1 de tests cliniques à cette époque.\
- Avril 2020 – Le candidat-vaccin Moderna a franchi une étape importante en passant à la deuxième phase de dosage.\
- Mai 2020 – Moderna a reçu l’autorisation de la FDA pour passer aux essais de phase II.\
- Juin 2020 – Le nombre de vaccins en cours de développement est passé à plus de 130, avec 16 dans les essais cliniques.\
- Juillet 2020 – Début de l’essai clinique de phase III Moderna.\
- Décembre 2020 – Le vaccin Moderna a reçu une autorisation d’utilisation d’urgence de la FDA, suivie rapidement des approbations EUA pour les vaccins Pfizer BioNTech et Johnson & Johnson.\
- Mai 2021 – La communauté mondiale a atteint l’étape majeure de 1 milliard de vaccins contre la COVID-19. Cet accomplissement stupéfiant est survenu quelques 4 mois seulement après le déploiement du vaccin et un peu plus d’un an après le début des essais de vaccins chez l’homme.
Solutions pour la découverte d’antigènes et d’immunogènes pour le développement de vaccins
Le développement de vaccins repose sur la compréhension initiale de l’ADN viral, des antigènes et de la réponse immunogène par le système immunitaire hôte. Dans la recherche sur les vaccins, les tests immunogènes sont utilisés dans les criblages viraux, suivis d’une caractérisation approfondie des gènes et protéines immunogènes positifs. Ils peuvent ensuite être mis au point et optimisés pour faciliter les efforts de développement de vaccins en aval. Les étapes clés du processus incluent l’utilisation d’outils pour le criblage et l’identification de clones cellulaires positifs.
https://share.vidyard.com/watch/VMz74R2JyixorrzhW1Pank
Dans cette vidéo, Justin Dranschack, directeur, plateforme BioPharma, passe en revue notre solution de flux du travail de développement d’un vaccin en utilisant des protéines recombinantes comme immunogène, et mentionne les systèmes pouvant vous aider dans vos recherches.
400 Les systèmes de repiquage de colonies microbiennes QPix® Series vous permettent d’automatiser entièrement les flux de travail de biologie de synthèse pour l’assemblage d’ADN, la détection d’anticorps et l’ingénierie des protéines. Proposant une gamme d'outil pour vos tests et pour le suivi de vos données, le logiciel QPix optimise le contrôle et la gestion des processus complexes et itératifs.
Le lecteur de microplaques multimode SpectraMax® i3x mesure l’absorbance, la fluorescence et la luminescence grâce à des mises à niveau disponibles, notamment le Western Blot , l’imagerie cellulaire et la cinétique rapide avec injecteurs, ainsi que des modes de détection supplémentaires.
Nos systèmes d’imagerie haut contenu ImageXpress offrent une solution de bout en bout pour le criblage et l’analyse haut contenu. Tous nos systèmes prennent en charge une large plage d’applications et offrent un débit élevé et des flux de travail optimisés.
3. Découverte d’anticorps : La course au développement et à la mise à l’échelle d’anticorps thérapeutiques
Bien que les efforts de développement de vaccins ciblent la prévention des infections virales et de la propagation, l’avènement des agents thérapeutiques pour traiter les maladies est tout aussi important. Le développement d’anticorps monoclonaux thérapeutiques a joué un rôle essentiel dans le renforcement du système immunitaire et l’assistance aux patients atteints de COVID-19. Le processus dépend de l’identification et de la caractérisation des anticorps, de l’ingénierie des protéines, de la sélection et de la croissance des lignées cellulaires d’hybridomes positifs.

- Avril 2020 – Plus de 150 médicaments étaient en cours de développement pour le traitement de la COVID-19, dont beaucoup avaient été précédemment approuvés pour d’autres infections virales et étaient indiqués comme sûrs pour l’usage humain. À l’heure actuelle, selon l’Organisation mondiale de la Santé, il y avait plus de études cliniques en 1 000 cours sur les traitements contre la COVID-19, dont beaucoup impliquaient des anticorps thérapeutiques.\
- Mai 2020 – Des essais cliniques de phase II et III ont été menés pour le nouvel anticorps polyclonal entièrement humain SAB-185, développé par SAB Biotherapeutics.\
- Juillet 2020 – Regeneron a participé à des essais cliniques de phase III pour un cocktail d’anticorps entièrement humanisé REGN-COV2, contenant deux anticorps qui se lient de manière non compétitive au domaine de liaison au récepteur de la protéine spike (S) du virus. Cet arrangement réduit la capacité des virus mutants à éviter le traitement et protège contre les variants de spicule qui ont évolué dans la population humaine.\
- Septembre 2020 – Il a été démontré que les données de l'essai de phase III pour le cocktail d'anticorps REGN-COV2 réduisent les charges virales et améliorent les systèmes des patients non hospitalisés atteints de COVID-19.\
- Décembre 2020 – La FDA a délivré sa première autorisation d’utilisation d’urgence pour un traitement par anticorps anti-COVID-19. Le bamlanivimab (de Eli Lilly) utilise des anticorps artificiellement conçus à partir de ceux isolés de personnes qui se sont rétablies de la maladie ou de patients en convalescence.\
- Mai 2021 – Avec l’approbation EUA de la FDA pour le nouvel anticorps Sotrovimab, les entreprises ont commencé à concevoir des anticorps de nouvelle génération modélisés sur ceux prélevés sur des individus uniques dont le système immunitaire peut neutraliser le SARS-CoV-2, y compris les nouveaux variants qui peuvent survenir.
Génération d’hybridomes et criblage de vastes bibliothèques d’anticorps
La technologie d’hybridome est une méthode pour la production en masse d’anticorps dans une lignée cellulaire hybride générée à partir de la fusion de cellules B productrices d’anticorps avec une lignée cellulaire de myélome immortalisée, appelée cellule d’hybridome. Étant donné que chaque cellule B produit un anticorps unique, le clonage de cellules uniques d’hybridomes peut être utilisé pour générer une bibliothèque diversifiée d’anticorps monoclonaux uniques à grande échelle, qui est fréquemment utilisée dans la prévention, le diagnostic et le traitement des maladies.
La vidéo ci-dessous présente notre solution pour un flux de travail sur les hybridomes et fait référence aux systèmes pour faciliter vos recherches.
https://share.vidyard.com/watch/XT7k1HMuRMAyrUUh5S75A774R2JyixorrzhW1Pank
Justin Dranschack, responsable des solutions biopharmaceutiques chez Molecular Devices, discute du flux de travail des AcM pour hybridomes et met en avant les systèmes automatisés qui accélèrent la mise sur le marché.
L’imageur CloneSelect® peut vous aider à répondre aux exigences réglementaires de la vérification des cellules uniques grâce à son analyse automatisée des cellules dans le canal de lumière blanche et à la fluorescence facultative pour ajouter une autre couche de confiance à la vérification de monoclonalité. Le système permet également des études de confluence et de monoclonalité simultanées.
Le système de repiquage de colonies de cellules de 2 mammifères ClonePix® est un système entièrement automatisé pour la sélection de clones de grande valeur utilisés dans la détection d’anticorps et le développement de lignées cellulaires. Disponible avec la fonction d’assurance de monoclonalité en option pour condenser les flux de travail de développement de lignées cellulaires en un seul instrument.
Les lecteurs de microplaques multimode SpectraMax® iD3 et iD5 mesurent l’absorbance, la fluorescence et la luminescence. En outre, le lecteur iD5 mesure la TRF et la FP et peut être étendu pour inclure la TR-FRET, la HTRF®, le BRET, les tests à gène rapporteur Dual-Luciferase avec injecteurs, ainsi que la détection par immunotransfert.
Nos systèmes d’imagerie haut contenu ImageXpress offrent une solution de bout en bout pour le criblage et l’analyse haut contenu. Tous nos systèmes prennent en charge une large plage d’applications et offrent un débit élevé et des flux de travail optimisés.
4. Comment accélérer vos recherches sur la COVID-19
Les flux de travail de développement de vaccins varient en fonction de la plateforme (p. ex., virus inactivé vs. vaccin à ADN) choisie, chacun ayant ses propres avantages. Augmenter la probabilité de succès contre l’agent infectieux, la CEPI, la Coalition for Epidemic Preparedness Innovations et de nombreuses autres organisations encouragent des approches diverses pendant une pandémie.
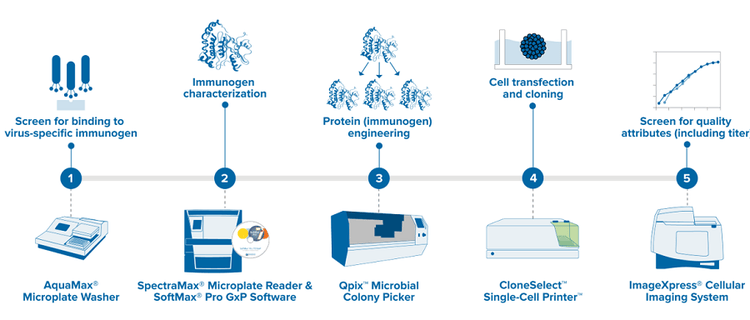
Nous avons créé divers flux de travail liés aux virus, allant de la détection d’antigènes/immunogènes et d’anticorps au développement de lignées cellulaires stables. Vous trouverez ci-dessus un flux de travail général pour le développement de vaccins utilisant des protéines recombinantes comme immunogène, faisant référence à des instruments automatisés pour accélérer vos recherches.